El mieloma múltiple
La informació proporcionada a www.fcarreras.org serveix per donar suport a la relació que existeix entre els pacients/visitants d’aquest lloc web i del seu metge, però no per reemplaçar-la.

Santi, 52 anys.
Mieloma múltiple.
“L’abril del 2021 em van detectar un mieloma múltiple després de més d’un any amb anèmia persistent. El diagnòstic d’un càncer incurable, i per tant crònic, com és el mieloma múltiple, és com un gerro d’aigua gelada que et cau a sobre. Ningú es pot imaginar que algun dia li tocarà la loteria de tenir un càncer. És difícil assimilar a la ment tota la informació que vas rebent per part dels metges.
Són dies foscos, amb angoixa, por, tristesa, també ràbia contra tot i contra tots, incomprensió, inquietuds… El futur tal com el coneixem fins ara desapareix. Toca passar doncs pel tractament inicial (combinació de medicaments durant 6/7 mesos, afèresi i auto trasplantament medul·lar). Cada fase amb necessitats i problemàtiques diferents. Aprens a centrar-te en cada etapa, cada dia, perquè les situacions són canviants. És evident que tot plegat et limita la vida, tant la personal com la laboral i com no, la familiar. Toca doncs adaptar-se a aquesta situació nova, reinventar-se ja que el Santi d’abans del mieloma múltiple ja no tornarà i cal abraçar-lo. M’agradaria acabar amb una frase que m’agrada molt i que em dona molta força: un no sap com pot ser de forta, quan ser fort és l’única opció que té”.
Informació revisada pel Dr. Albert Oriol. Membre del Servei d’Hematologia de l’Institut Català d’Oncologia – Badalona. Investigador de l’Institut d’Investigació contra la Leucèmia Josep Carreras. Col·legi de Metges de Barcelona (Col. 26696).
Com funciona la medul·la òssia i quins són els tipus de cèl·lules sanguínies?
El mieloma múltiple (MM) és un tipus de càncer de les cèl·lules de la sang que s’origina a la medul·la òssia. Vegeu apartat Leucèmia, medul·la òssia i cèl·lules sanguínies.
Què és el mieloma múltiple i a qui afecta?
El mieloma múltiple és una malaltia de la medul·la òssia, en concret de les cèl·lules plasmàtiques, com la resta de gammapaties monoclonals.
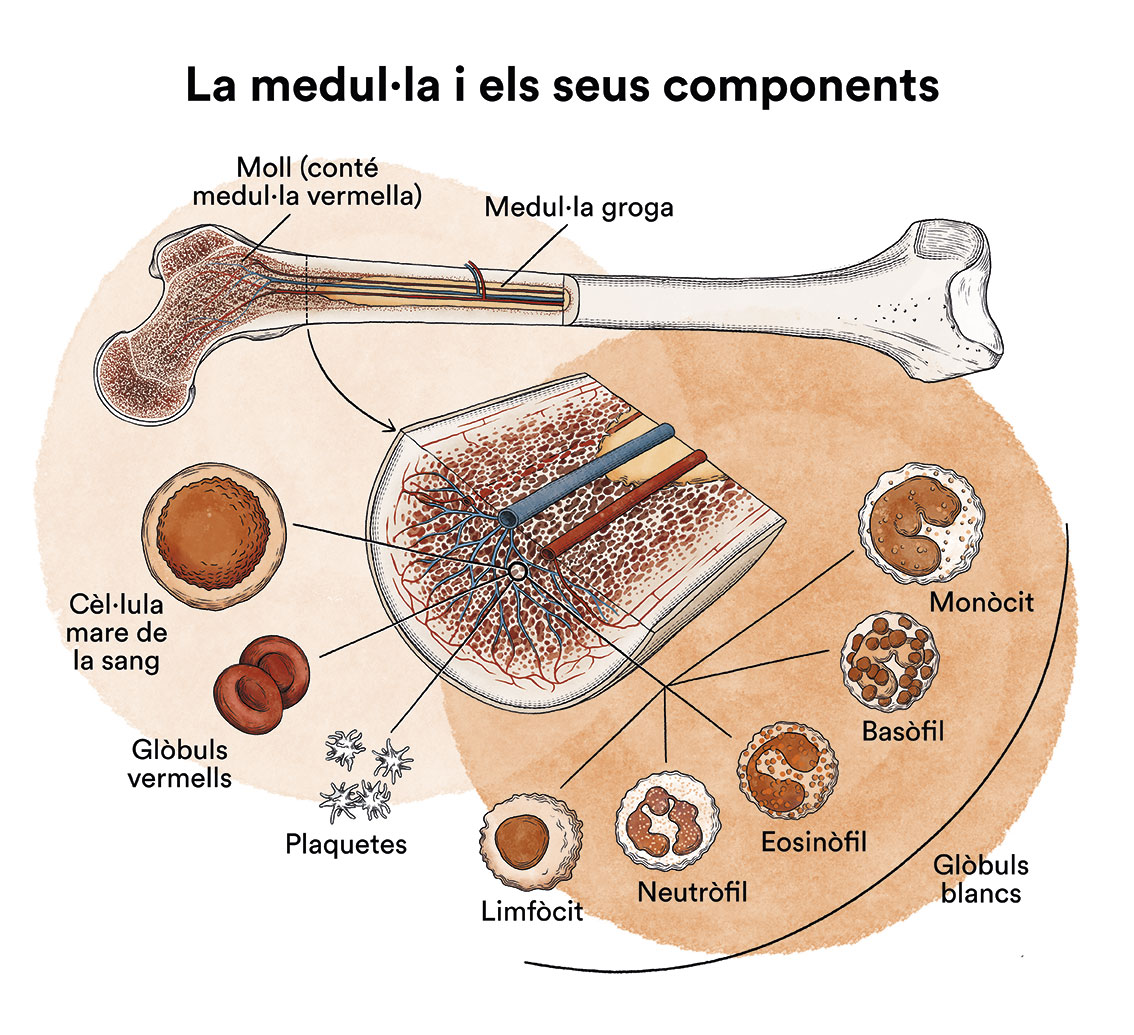
Les cèl·lules plasmàtiques normals formen part del sistema immunològic o de defensa de l’organisme, i són les encarregades de fabricar les immunoglobulines, unes proteïnes capaces d’atacar gèrmens davant una infecció. En condicions normals, les cèl·lules plasmàtiques madures fabriquen durant tota la seva existència un únic tipus d’immunoglobulina i no es reprodueixen.
Determinades alteracions genètiques poden fer que les cèl·lules plasmàtiques recuperin la capacitat de reproduir-se i ocupar parcialment la medul·la òssia. Aquesta situació no sempre produeix trastorns clínics: quan aquest procés és asimptomàtic, parlem de gammapatia monoclonal de significat incert (GMSI) o de mieloma quiescent (MMq). Les persones en les qui es detecta una GMSI o un MMq no necessiten tractament, però sí que han de ser controlades periòdicament, ja que existeix el risc que acabin desenvolupant un mieloma múltiple (MM) actiu.
A Europa, es diagnostiquen aproximadament 40 nous casos de MM per cada milió d’habitants i any. A l’Estat espanyol això suposa uns 3.000 nous diagnòstics cada any. El mieloma apareix característicament a gent gran, més de la meitat dels pacients es diagnostiquen més enllà dels 65 o 70 anys, tot i que pot afectar també adults joves.
Quines són les causes del mieloma múltiple?
No existeix cap factor conegut que sigui causa directa de l’aparició del mieloma múltiple. Factors que augmenten el risc d’altres neoplàsies com ara les radiacions, els virus, el tabac o l’alcohol no sembla que tinguin cap relació amb aquesta malaltia. Els precursors de les cèl·lules plasmàtiques pateixen alteracions genètiques programades en el gangli durant el seu procés d’“especialització”. Possiblement, errors en aquests canvis genètics són l’origen del desenvolupament de famílies de cèl·lules plasmàtiques anòmales que s’instal·laran a la medul·la òssia més endavant. De moment no s’ha identificat cap virus o element tòxic que faciliti aquestes mutacions genètiques errònies, i tampoc no sabem per què en algunes persones aquestes alteracions duen al desenvolupament d’una GMSI. L’únic que és segur és que mai no progressarà a mieloma, mentre que, en altres, el pas de GMSI a MM és molt ràpid.
El mieloma múltiple no és contagiós.
Vegeu apartat Leucèmia, medul·la òssia i cèl·lules sanguínies.
Quins són els símptomes del mieloma múltiple?
La freqüència amb la que ens fem anàlisis de rutina en l’actualitat fa que cada cop sigui més habitual diagnosticar un mieloma múltiple (MM) quan encara és asimptomàtic; per exemple, durant els controls d’una GMSI detectada casualment.
El símptoma més freqüent del mieloma múltiple (MM) és el dolor ossi, sobretot a la columna vertebral, les costelles i el maluc. El MM provoca lesions en els ossos anomenades “lesions lítiques”, zones de l’os que perden el seu contingut en calci i es debiliten. Aquestes lesions acostumen a ser molt doloroses i, si són prou importants, poden provocar també una fractura de l’os afectat, la qual cosa es percep com a un dolor intens d’aparició brusca. De vegades, el primer símptoma del mieloma és un aixafament vertebral en aixecar un pes no especialment gran o una fractura després d’un cop banal.
El segon símptoma més freqüent en el mieloma múltiple és l’anèmia. Les cèl·lules del mieloma envaeixen la medul·la òssia i fabriquen substàncies que impedeixen la fabricació normal de glòbuls vermells: això produeix anèmia, que es percep habitualment com a cansament, manca d’energia i fatiga en esforços cada vegada més lleus. L’anèmia també pot sospitar-se per pal·lidesa de la pell, de les ungles o la conjuntiva ocular.
Tot i que el dolor i l’anèmia són els dos símptomes més freqüents del mieloma múltiple, cal tenir en compte que el dolor i la fatiga són dos símptomes molt comuns en una gran varietat de malalties, incloses les infeccions víriques i bacterianes, o les malalties reumàtiques. Per una banda, en persones d’edat avançada, el motiu més freqüent de dolor ossi són els trastorns degeneratius, principalment l’artrosi. D’altra banda, les causes més freqüents de fatiga són els problemes cardíacs o respiratoris, molt més freqüents que el mieloma múltiple.
En tot cas, davant problemes de dolor difícils de controlar amb analgèsics o davant una fatiga persistent que augmenta amb el temps, és important fer una anàlisi general, incloent-hi una determinació de proteïnes. En més del 95 % dels casos de mieloma múltiple és fàcil observar proteïnes anòmales en sang o en orina (el que es coneix com a el component o banda monoclonal), que servirà alhora per orientar el diagnòstic i per fer un seguiment de la resposta al tractament.
Hi ha altres símptomes que apareixen amb menys freqüència, però que són molt importants perquè poden requerir tractament específic i ens fan sospitar ràpidament d’un mieloma múltiple i, per tant, instaurar un tractament adequat. Els dos principals són la hipercalcèmia, augment del calci en sang, que presenten un 13 % dels pacients en el diagnòstic, o la insuficiència renal, present en un 19 % dels pacients. La insuficiència renal i la hipercalcèmia es detecten en anàlisis de sang bàsiques. Les seves manifestacions clíniques són poc específiques: manca de l’apetit, somnolència, manca d’energia o restrenyiment, però poden produir símptomes més alarmants com ara nàusees i vòmits o somnolència, que pot arribar a l’estupor i al coma. En aquests casos, l’habitual és buscar atenció urgent. En una anàlisi bàsica d’urgències s’identificarà el problema amb facilitat. Tant la insuficiència renal com la hipercalcèmia requereixen tractament immediat, tot i que el MM no estigui encara diagnosticat.
És molt estrany que el mieloma provoqui febre, tot i que és molt freqüent que el mieloma es diagnostiqui a la mateixa vegada que una infecció. De fet, és important sospitar un trastorn de la immunitat en general en una persona que ha patit més d’una infecció greu en pocs mesos, sobretot si no té cap malaltia coneguda que ho justifiqui.
El mieloma també es pot manifestar com a un bony o tumor de consistència dura que normalment creix a partir d’una zona d’os com ara el crani, una costella o l’estern. Quan aquestes masses s’originen a les vèrtebres no solen ser visibles o palpables, ja que acostumen a créixer cap a l’interior, però poden provocar la compressió de la medul·la espinal o les arrels dels nervis que surten d’aquesta medul·la. Això dona manifestacions greus, com ara la pèrdua de força o de sensibilitat de les cames, o la pèrdua de control dels esfínters (retenció d’orina). Aquestes manifestacions són relativament poc freqüents, però, si es donen, s’ha de buscar atenció mèdica urgent.
Altres vegades el MM pot trigar en diagnosticar-se, sobretot perquè amb freqüència els símptomes inicials són poc alarmants o fàcilment atribuïbles a altres causes (mal d’esquena, cansament…). Tot i això, és important sospitar la presència d’un mieloma davant un dolor que no es controla amb tractaments analgèsics habituals. Un aixafament vertebral, per exemple, tot i que es produeixi en una persona gran, ha de dur a realitzar un estudi bàsic incloent almenys una analítica bàsica i proves radiològiques. Si en l’anàlisi sanguínia hi ha anèmia, proteïnes per sobre dels nivells normals, alteració de la funció renal o augment del calci en sang, el MM s’ha de sospitar sempre. També s’ha de sospitar un MM si les radiografies demostren “lesions lítiques”, típiques de la malaltia, o fractures no causades per un traumatisme previ.

Joan
Mieloma múltiple.
“El octubre del 2013 vaig ingressar d’urgències amb una insuficiència renal severa, deshidratació, febre,… Al cap de pocs dies em van diagnosticar mieloma múltiple. Mai no havia sentit aquest nom, però sí la paraula quimio. En aquell moment, com a tots, se’m va venir el món a sobre i vaig plorar. A l’agost de l’any següent, finalment va arribar l’autotrasplantament que va ser un èxit i aquí estic… amb les meves seqüeles, infeccions diverses… però amb ganes de viure i agrair aquesta oportunitat brindada”.
Com es diagnostica el mieloma múltiple?
Quan existeix la sospita, el diagnòstic de mieloma múltiple és relativament senzill. S’han de realitzar dues proves essencials:
- Una anàlisi completa de proteïnes en sang i en orina que permeti caracteritzar correctament el component monoclonal
- Un mielograma o aspirat de medul·la òssia per confirmar la presència de cèl·lules plasmàtiques anormals a la medul·la òssia. En aquest aspirat medul·lar s’ha d’obtenir un nombre de cèl·lules suficient per realitzar estudis genètics (hi ha alteracions genètiques de pitjor pronòstic que interessa detectar) i estudis de citometria de flux (per identificar característiques de les cèl·lules del mieloma que facilitin el seguiment de la malaltia residual després del tractament.
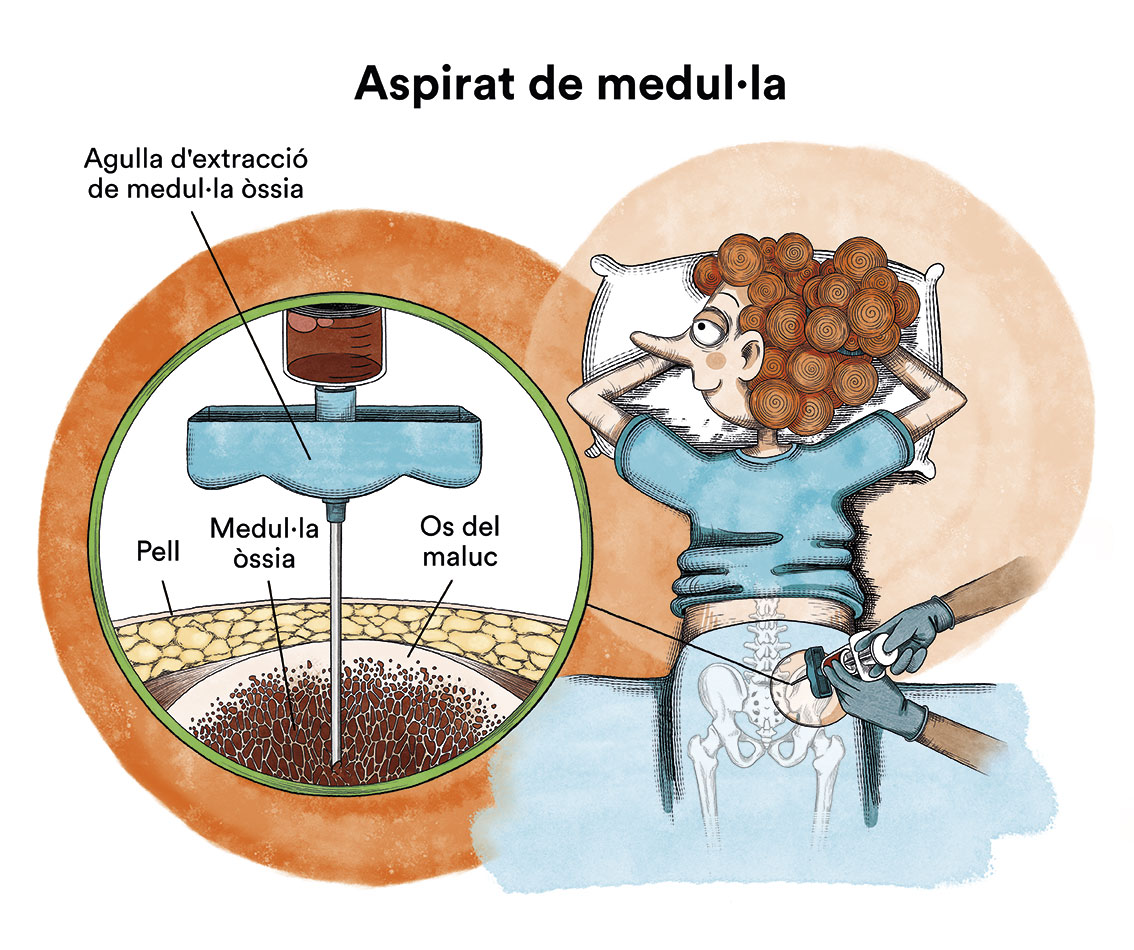
A més, és important completar el diagnòstic amb altres proves importants per determinar el pronòstic i dirigir l’actitud terapèutica, que són bàsicament proves d’imatge:
S’ha de determinar bé el nombre i localització de les lesions òssies mitjançant un estudi radiològic de tot l’esquelet. La tomografia (TC) permet veure lesions en zones on la radiografia simple és poc sensible, la ressonància magnètica permet avaluar millor la columna i és especialment útil si se sospita compressió medul·lar o masses de mieloma (plasmocitomes) al costat de les vèrtebres, i la tomografia d’emissió de positrons (PET-TC) pot detectar lesions en altres localitzacions, tot i que no sempre és necessari fer totes aquestes proves.
El mieloma és una malaltia disseminada que afecta tot l’esquelet. Per tant, a diferència d’altres càncers, l’estadificació (basada en variables com ara la quantitat de component monoclonal en sang i en orina, lesions òssies, presència d’anèmia i nivell de calci en sang), no serveix per distingir malaltia localitzada de malaltia disseminada. El mesurament de dos paràmetres en sang (albúmina i beta2-microglobulina) permet classificar els mielomes en tres estadis amb diferent “quantitat de mieloma” i amb diferent pronòstic.
Quin és el tractament del mieloma múltiple?
Els primers tractaments per al mieloma daten dels anys seixanta i es basaven en la combinació de corticoides amb un grup d’agents quimioteràpics anomenats alquilants. Aquests fàrmacs continuen formant part indispensable del tractament del mieloma, però des de finals del segle passat, l’addició d’altres fàrmacs ha canviat de forma molt important el pronòstic de la malaltia. Aquests nous fàrmacs pertanyen sobretot a dues famílies, els anomenats “immunomoduladors” (talidomida, lenalidomida, pomalidomida) i els “inhibidors del proteasoma” (bortezomib, carfilzomib, ixazomib). No es consideren agents quimioteràpics en el sentit convencional de la paraula, fet que no vol dir que no tinguin també alguns efectes no desitjables.
En general, cap d’aquests fàrmacs s’utilitza de forma aïllada, ja que el seu ús combinat dificulta que el mieloma múltiple desenvolupi resistències i permet un control més ràpid dels símptomes. En general, un tractament més intens i més prolongat amb una combinació de fàrmacs es tradueix en una eficàcia més elevada i una durada més llarga de la resposta. Tot i això, la intensitat i durada del tractament s’han de modular per evitar un excés de toxicitat. La individualització del tractament, per tant, dependrà de la capacitat del pacient per tolerar tractaments més o menys intensius. En aquest sentit, l’edat és un factor molt rellevant, tot i que no és l’únic que cal considerar.

En pacients relativament joves (fins als 65 o 70 anys) i amb un estat general adequat, s’intenta un tractament el més intensiu possible, inclòs un trasplantament autòleg de progenitors de medul·la òssia. El motiu d’això és que els alquilants (i en concret, l’alquilant que s’utilitza habitualment per al mieloma, el melfalan) són molt tòxics per a les cèl·lules de la medul·la òssia. Utilitzar melfalan en dosis molt altes implica augmentar la seva eficàcia però també destruir de forma irreversible molta cel·lularitat sana de la medul·la òssia i, per tant, per administrar altes dosis de malfalan és necessari recollir prèviament cèl·lules progenitores de la medul·la òssia, administrar les dosis altes de melfalan i posteriorment reinfondre cèl·lules sanes perquè les cèl·lules de la sang puguin recuperar-se.
En pacients joves i sense altres problemes de salut greus, un tractament estàndard podria ser una combinació d’immunomodulador, un inhibidor del proteasoma i un corticoide durant 4-6 cicles (tractament d’inducció), seguit d’altes dosis de melfalan amb trasplantament autòleg de progenitors i, si és possible, afegir encara més tractament després del trasplantament (tractaments de consolidació o de manteniment). Així els règims més freqüentment utilitzats a l’Estat espanyol són VTD (bortezomib, talidomida, dexametasona), VRD (bortezomib, lenalidomida i dexametasona) i VCD (on s’utilitza ciclofosfamida en comptes d’un immunomodulador). Ja hi ha aprovació per a una teràpia quàdruple en què s’inclou un anticòs denominat daratumumab (dirigit a CD38, que és una molècula expressada en les cèl·lules plasmàtiques) juntament amb VTD i que acabarà substituint els règims anteriors en els pacients candidats a trasplantament i sense contraindicacions.
En pacients en els qui un trasplantament no sigui aconsellable per la seva excessiva toxicitat, s’acostuma a utilitzar una combinació de tres fàrmacs, que pot incloure també melfalan tot i que en dosis més baixes, o combinacions de només dos fàrmacs, incloent-hi sempre un inhibidor del proteasoma, un immunomodulador o els dos. En tot cas, el tractament s’ha d’adaptar a la fragilitat del pacient per evitar un excés de toxicitat: es pot intentar mantenir els tractaments amb dos fàrmacs o bé amb tres fàrmacs a dosis reduïdes o espaiades de forma continuada i, amb això, obtenir resultats propers als obtinguts amb tractaments més intensius.
El tractament de les recaigudes també acostuma a ser una combinació de dos o tres fàrmacs. Per a la tria del tractament, és important considerar: la resposta als tractaments previs (es poden repetir tractaments administrats anteriorment, només si amb aquests tractaments es van aconseguir bons resultats), la toxicitat dels tractaments anteriors (cal evitar fàrmacs que ja van produir massa toxicitat), les característiques de la recaiguda i les opcions de tractament posteriors en cas de fracàs.
En conclusió, existeixen diversos fàrmacs útils per al tractament del mieloma múltiple, però és important individualitzar bé el tractament, en funció de l’edat i les característiques del pacient i de la malaltia.
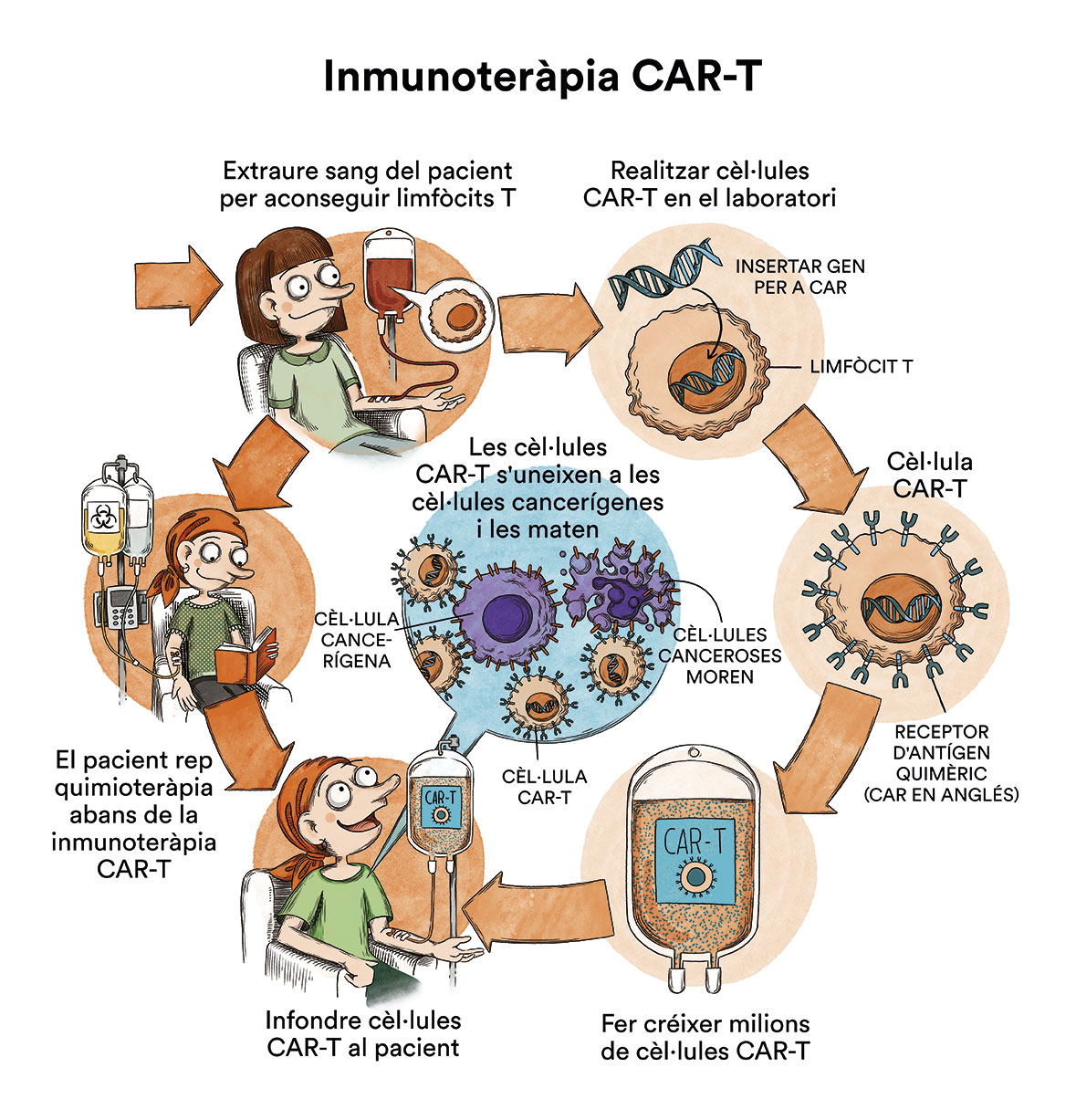
En els darrers anys també ha aparegut la immunoteràpia CART (contingut en espanyol), que avui dia també pot ser d’aplicació en certs pacients de mieloma múltiple seleccionats. L’idecabtagen vicleucel (ide-cel, Abecma) i el ciltacabtagen autoleucel (cilta-cel, Carvykti) són teràpies de cèl·lules CAR-T dirigides a la proteïna BCMA, la qual està present en les cèl·lules del mieloma múltiple. Aquests tractaments poden utilitzar-se en pacients que ja s’han sotmès a diversos tipus de tractaments (com a mínim, 4 generalment) per combatre el mieloma múltiple. Només poden administrar-se en centres de referència autoritzats per fer-ho.

Juanma
Mieloma múltiple.
“Em van diagnosticar un mieloma múltiple el 2018. Des d’aleshores m’he sotmès a sis línies de tractament que han anat fallant una darrere l’altra, però a la setena, després d’un tractament d’immunoteràpia CART, vaig sentir per primera vegada l’estrofa més meravellosa del món: Juanma, la malaltia està en remissió total. No hi ha rastre de cèl·lules tumorals. La malaltia està ara mateix controlada. Quan et diuen que estàs en remissió total no vol dir que estiguis curat perquè se suposa que el mieloma múltiple de moment és incurable i hi pot haver recaigudes, però soc més optimista que mai”.
Quin pronòstic tenen els pacients de mieloma múltiple?
El mieloma múltiple es considera encara una malaltia incurable. La majoria de pacients patiran recaigudes després del tractament inicial de la malaltia i necessitaran tornar a tractar-se, probablement en diverses ocasions. Això no vol dir que el pronòstic sigui molt dolent; de fet, és extremadament variable. Una petita proporció de pacients (fins un 10 %) tindran una excel·lent resposta al tractament de primera línia i és possible que no recaiguin mai. Anomenem aquests pacients “funcionalment curats”, ja que mai no tindrem la seguretat que el MM no reaparegui, tot i que hagin passat 10 o 15 anys sense malaltia. A l’altre extrem hi ha un 10-15 % de pacients que poden ser resistents al tractament inicial o bé respondre inicialment, però recaure molt aviat. El pronòstic vital en aquests casos és molt dolent, al voltant dels dos anys. Entre aquests dos extrems, la majoria dels pacients respondran adequadament al tractament inicial, els seus símptomes desapareixeran o milloraran molt després de les primeres setmanes de tractament, i no tindran un risc vital a curt o mig termini.
Tot i això, el pronòstic a llarg termini és més incert, ja que dependrà de la freqüència i agressivitat de les recaigudes. Inclús amb un pronòstic vital similar, pacients amb recaigudes poc agressives i bona tolerància als tractaments poden tenir una qualitat de vida excel·lent durant anys, mentre que d’altres amb recaigudes agressives o bé amb mala tolerància als diferents fàrmacs poden arrossegar seqüeles que la redueixin de forma important. Per tant, es tracta d’una malaltia amb un pronòstic molt variable, i tot i que bona part de l’estudi diagnòstic inicial s’encamina a intentar predir el tipus de MM al qual ens enfrontem, cap prova és adequada per anticipar un pronòstic exacte, ni en temps ni en qualitat de vida.
El comportament clínic inicial del MM i sobretot la resposta al primer tractament ens donarà molta informació pronòstica. En pacients que presentin una resposta molt duradora al primer tractament, la resposta al segon i successius tractaments acostuma a ser també bona, i és en aquests casos quan podem pensar en el MM com si es tractés d’una malaltia crònica. La situació és totalment diferent en pacients que després d’un tractament recauen molt aviat o recauen de forma molt brusca i requereixen un altre tractament de seguida. Les recaigudes brusques afavoreixen l’acumulació de seqüeles (especialment la insuficiència renal i les lesions òssies), i no només afecten la qualitat de vida, sinó que amb freqüència redueixen les opcions de tractament següents.
És important anticipar-se i evitar les seqüeles de la malaltia i els problemes relacionats amb la toxicitat dels tractaments realitzant un seguiment rigorós dels pacients amb MM, tant si estan rebent tractament actiu com en el temps en què no tenen símptomes.
Viure amb el mieloma múltiple: alimentació i assistència
Els tractaments per al mieloma tenen toxicitat, que s’ha de vigilar i prevenir, però no impedeixen dur una vida pràcticament normal. Hi ha dos aspectes que el pacient ha de vigilar especialment: les infeccions i les lesions òssies (contingut en espanyol).
Els pacients amb mieloma tenen un risc de patir infeccions 10 vegades més alt que la població sana. Aquest risc és més elevat quan el mieloma no està controlat, en l’etapa inicial de qualsevol tractament i sobretot en el mieloma avançat. Tot i això, en pacients que tenen el MM sota control i que no requereixen tractament en aquest moment, el risc d’infecció és superior al de la població sana. Les infeccions de les vies respiratòries són les més freqüents i també les potencialment més greus. El risc de patir una infecció no és prevenible, però certes mesures bàsiques ajuden a reduir el nombre d’episodis. Extremar la higiene, evitar el contacte directe amb familiars o persones amb processos infecciosos actius o evitar en la mesura que es pugui les aglomeracions en èpoques de grip és recomanable. En la transmissió per contacte, el rentat freqüent de mans és la mesura més important, en situacions especials (per exemple, sales d’espera d’hospitals) i en moments d’especial sensibilitat (per exemple, després d’un trasplantament) pot ser que se li recomani dur una mascareta per evitar gèrmens de transmissió per l’aire. Altres mesures senzilles són una nutrició equilibrada i variada (no són necessaris els compostos vitamínics ni suplements), una bona hidratació, exercici moderat (millor a l’aire lliure) i evitar el tabac o els ambients carregats.
Les lesions òssies causades pel MM es recuperen molt lentament i la fragilitat òssia s’ha de considerar com a permanent inclús després d’un tractament d’èxit. És important prevenir els aixafaments vertebrals, evitant aixecar o arrossegar pesos importants. L’exercici moderat reforça la musculatura i afavoreix la recalcificació òssia, però no són recomanables esports de contacte o que impliquin moviments bruscos i violents, pel risc de patir fractures. Tot i que un dels símptomes del mieloma és la hipercalcèmia (excés de calci en sang), els aliments rics en calci (formatges, lactis) estan clarament recomanats. El tractament del mieloma acostuma a incloure uns fàrmacs anomenats bifosfonats que ajuden l’os a recuperar-se, captant el calci del torrent sanguini. Per aquest motiu, als pacients amb mieloma en tractament amb bifosfonats se’ls recomana una dieta rica en calci o suplements de calci i vitamina D, ja que tenen amb molta més freqüència el calci sanguini baix.
Recomanem informar-se sobre com dur una alimentació sana durant el tractament (contingut en espanyol)? I sobre exercicis d’activitat física i fisioteràpia recomanats (Manual fisioteràpia en pacients onco-hematològics(contingut en espanyol)) i programa EnforMMA.
Enllaços d'interès sobre temes mèdics relacionats amb el mieloma múltiple
- Guia del Mieloma Múltiple del Grup espanyol del Mieloma, 2021
- Mieloma múltiple. AEAL
- Mieloma Múltiple. American Cancer Society
- Comunidad Española de Pacientes de Mieloma Múltiple
- Mieloma múltiple. Portal Clínic. Hospital Clínic de Barcelona.
- La guia sobre el mieloma: informació per a pacients i cuidadors. Leukemia & Lymphoma Society
Enllaços d'interès sobre altres temes relacionats amb el mieloma múltiple
MATERIALS TESTIMONIALS
Pots sol·licitar-nos els llibrets en format paper per a enviament gratuït a l’Estat espanyol a través del correu electrònic: imparables@fcarreras.es
TRASPLANTAMENT DE MEDUL·LA ÒSSIA
- Guia del Trasplantament de Medul·la Òssia. Fundació Josep Carreras (contingut en espanyol)
- Què és l’HLA i com funciona? Fundació Josep Carreras (contingut en espanyol)
- La Malaltia Empelt contra Receptor. Fundació Josep Carreras (contingut en espanyol)
- Història del Trasplantament de Medul·la Òssia. Fundació Josep Carreras (contingut en espanyol)
- Com es realitza la cerca d’un donant compatible anònim? Fundació Josep Carreras (contingut en espanyol)
ALIMENTACIÓ
- Com mantenir una alimentació saludable durant el tractament? Fundació Josep Carreras (contingut en espanyol)
- Guia de nutrició. Leukemia & Lymphoma Society
ALTRES
- Guia pràctica sobre mieloma múltiple per a pacients i cuidadors. Fundació Josep Carreras contra la leucèmia
- Idees sobre què emportar-me a una cambra d’aïllament. Fundació Josep Carreras contra la leucèmia (contingut en espanyol)
- Consells de viatge per a persones amb càncer. Fundació Josep Carreras contra la leucèmia (contingut en espanyol)
- Manual de fisioteràpia en pacients hematològics i trasplantats. Fundació Josep Carreras contra la leucèmia (contingut en espanyol)
- Prevenció i tractament de la mucositis oral. Fundació Josep Carreras contra la leucèmia (contingut en espanyol)
- La higiene bucodental en el pacient onco-hematològic. Fundació Josep Carreras contra la leucèmia (contingut en espanyol)
- Manual fertilitat: Patir un càncer de la sang i ser pare o mare. Fundació Josep Carreras contra la leucèmia (contingut en espanyol)
- La cura de la pell en el pacient onco-hematològic. Fundació Josep Carreras contra la leucèmia (contingut en espanyol)
- Manual Estètica Oncològica. Fundació Josep Carreras contra la leucèmia (contingut en espanyol)
- Leucèmia i sexualitat. Fundació Josep Carreras contra la leucèmia (contingut en espanyol)
- 7 formes de posar-se un mocador. Fundació Josep Carreras contra la leucèmia (contingut en espanyol)
Enllaços d'interès: entitats locals/provincials o estatals que poden proveir-te de recursos i serveis especialitzats en leucèmia o en pacients oncològics:
A l’Estat espanyol existeix un gran teixit associatiu per a pacients amb càncer hematològic que, en molts casos, poden informar-te, assessorar-te i fins i tot realitzar alguns tràmits. Aquests són els contactes d’algunes de les associacions per Comunitats Autònomes:
Totes aquestes organitzacions són externes a la Fundació Josep Carreras.
ESTATAL
- CEMMP (Comunidad Española de Pacientes de Mieloma Múltiple)
- AEAL (ASOCIACIÓN ESPAÑOLA DE AFECTADOS POR LINFOMA, MIELOMA y LEUCEMIA)
- AECC (ASOCIACIÓN ESPAÑOLA CONTRA EL CÁNCER). Present a les diferents províncies i a moltes localitats. Contactar amb la seu més propera o trucant al 900 100 036 (24h).
- AELCLES (Agrupación Española contra la Leucemia y Enfermedades de la Sangre)
- FUNDACIÓ JOSEP CARRERAS CONTRA LA LEUCÈMIA
- FUNDACIÓ SANDRA IBARRA
- GEPAC (GRUPO ESPAÑOL DE PACIENTES CON CÁNCER)
- MPN España (Asociación de Afectados Por Neoplasias Mieloproliferativas Crónicas)
ANDALUSIA
- AECC (ASOCIACIÓN ESPAÑOLA CONTRA EL CÁNCER). Present a les diferents províncies i a moltes localitats. Contactar amb la seu més propera.
- ALUSVI (ASOCIACIÓN LUCHA Y SONRÍE POR LA VIDA). Sevilla
- APOLEU (ASOCIACIÓN DE APOYO A PACIENTES Y FAMILIARES DE LEUCEMIA). Cadis
ARAGÓ
- AECC (ASOCIACIÓN ESPAÑOLA CONTRA EL CÁNCER). Present a les diferents províncies i a moltes localitats. Contactar amb la seu més propera.
- ASPHER (ASOCIACIÓN DE PACIENTES DE ENFERMEDADES HEMATOLÓGICAS RARAS DE ARAGÓN)
- DONA MÉDULA ARAGÓN
ASTÚRIES
- AECC (ASOCIACIÓN ESPAÑOLA CONTRA EL CÁNCER). Present a les diferents províncies i a moltes localitats. Contactar amb la seu més propera.
- ASTHEHA (ASOCIACIÓN DE TRASPLANTADOS HEMATOPOYÉTICOS Y ENFERMOS HEMATOLÓGICOS DE ASTURIAS)
CANTÀBRIA
- AECC (ASOCIACIÓN ESPAÑOLA CONTRA EL CÁNCER). Present a les diferents províncies i a moltes localitats. Contactar amb la seu més propera.
CASTELLA-LA MANXA
- AECC (ASOCIACIÓN ESPAÑOLA CONTRA EL CÁNCER). Present a les diferents províncies i a moltes localitats. Contactar amb la seu més propera.
CASTELLA I LLEÓ
- ABACES (ASOCIACIÓN BERCIANA DE AYUDA CONTRA LAS ENFERMEDADES DE LA SANGRE)
- AECC (ASOCIACIÓN ESPAÑOLA CONTRA EL CÁNCER). Present a les diferents províncies i a moltes localitats. Contactar amb la seu més propera.
- ALCLES (ASOCIACIÓN LEONESA CON LAS ENFERMEDADES DE LA SANGRE). Lleó.
- ASCOL (ASOCIACIÓN CONTRA LA LEUCEMIA Y ENFERMEDADES DE LA SANGRE). Salamanca.
CATALUNYA
- ASSOCIACIÓ FÈNIX. Solsona
- FECEC (FEDERACIÓ CATALANA D’ENTITATS CONTRA EL CÀNCER
- FUNDACIÓ KÁLIDA. Barcelona
- FUNDACIÓ ROSES CONTRA EL CÀNCER. Roses
- LLIGA CONTRA EL CÀNCER COMARQUES DE TARRAGONA I TERRES DE L’EBRE. Tarragona
- MielomaCAT
- ONCOLLIGA BARCELONA. Barcelona
- ONCOLLIGA GIRONA. Girona
- ONCOLLIGA COMARQUES DE LLEIDA. Lleida
- ONCOVALLÈS. Vallès Oriental
- OSONA CONTRA EL CÀNCER. Osona
- SUPORT I COMPANYIA. Barcelona
- VILASSAR DE DALT CONTRA EL CÀNCER. Vilassar de Dalt
COMUNITAT VALENCIANA
- AECC (ASOCIACIÓN ESPAÑOLA CONTRA EL CÁNCER). Present a les diferents províncies i a moltes localitats. Contactar amb la seu més propera.
- ASLEUVAL (ASOCIACIÓN DE PACIENTES DE LEUCEMIA, LINFOMA, MIELOMA Y OTRAS ENFERMEDADES DE LA SANGRE DE VALENCIA)
EXTREMADURA
- AECC (ASOCIACIÓN ESPAÑOLA CONTRA EL CÁNCER). Present a les diferents províncies i a moltes localitats. Contactar amb la seu més propera.
- AFAL (AYUDA A FAMILIAS AFECTADAS DE LEUCEMIAS, LINFOMAS; MIELOMAS Y APLASIAS)
- AOEX (ASOCIACIÓN ONCOLÓGICA EXTREMEÑA)
GALÍCIA
- AECC (ASOCIACIÓN ESPAÑOLA CONTRA EL CÁNCER). Present a les diferents províncies i a moltes localitats. Contactar amb la seu més propera.
- ASOTRAME (ASOCIACIÓN GALLEGA DE AFECTADOS POR TRASPLANTES MEDULARES)
ILLES BALEARS
- ADAA (ASSOCIACIÓ D’AJUDA A L’ACOMPANYAMENT DEL MALALT DE LES ILLES BALEARS)
- AECC (ASOCIACIÓN ESPAÑOLA CONTRA EL CÁNCER). Present a les diferents províncies i a moltes localitats. Contactar amb la seu més propera.
ILLES CANÀRIES
- AECC (ASOCIACIÓN ESPAÑOLA CONTRA EL CÁNCER). Present a les diferents províncies i a moltes localitats. Contactar amb la seu més propera.
- AFOL (ASOCIACIÓN DE FAMILIAS ONCOHEMATOLÓGICAS DE LANZAROTE)
- FUNDACIÓ ALEJANDRO DA SILVA
LA RIOJA
- AECC (ASOCIACIÓN ESPAÑOLA CONTRA EL CÁNCER). Present a les diferents províncies i a moltes localitats. Contactar amb la seu més propera.
MADRID
- AECC (ASOCIACIÓN ESPAÑOLA CONTRA EL CÁNCER). Present a les diferents províncies i a moltes localitats. Contactar amb la seu més propera.
- AEAL (ASOCIACIÓN ESPAÑOLA DE LEUCEMIA Y LINFOMA)
- CRIS CONTRA EL CÁNCER
- FUNDACIÓN LEUCEMIA Y LINFOMA
MÚRCIA
- AECC (ASOCIACIÓN ESPAÑOLA CONTRA EL CÁNCER). Present a les diferents províncies i a moltes localitats. Contactar amb la seu més propera.
NAVARRA
- AECC (ASOCIACIÓN ESPAÑOLA CONTRA EL CÁNCER). Present a les diferents províncies i a moltes localitats. Contactar amb la seu més propera.
PAÍS BASC
- AECC (ASOCIACIÓN ESPAÑOLA CONTRA EL CÁNCER). Present a les diferents províncies i a moltes localitats. Contactar amb la seu més propera.
- PAUSOZ-PAUSO. Bilbao
CIUTATS AUTÒNOMES DE CEUTA I MELILLA
- AECC CEUTA (ASOCIACIÓN ESPAÑOLA CONTRA EL CÁNCER)
- AECC MELILLA (ASOCIACIÓN ESPAÑOLA CONTRA EL CÁNCER)
Suport i ajuda
Et convidem també a seguir-nos a través de les nostres xarxes socials principals (Facebook, Twitter e Instagram) on sovint compartim testimonis de superació.
Si resideixes a l’Estat espanyol, també pots posar-te en contacte amb nosaltres enviant-nos un correu electrònic a imparables@fcarreras.es perquè t’ajudem a posar-te en contacte amb altres famílies que han superat aquesta malaltia.
* D’acord amb la Llei 34/2002 de Serveis de la Societat de la Informació i el Comerç Electrònic (LSSICE), la Fundació Josep Carreras contra la Leucèmia informa que tota la informació mèdica disponible a www.fcarreras.org ha estat revisada i acreditada pel Dr. Enric Carreras Pons, Col·legiat núm. 9438, Barcelona, Doctor en Medicina i Cirurgia, Especialista en Medicina Interna, Especialista en Hematologia i Hemoteràpia i Consultor sènior de la Fundació; i per la Dra. Rocío Parody Porras, Col·legiada núm. 35205, Barcelona, Doctora en Medicina i Cirurgia, Especialista en Hematologia i Hemoteràpia i adscrita a la Direcció mèdica del Registre de Donants de Medul·la Òssia (REDMO) de la Fundació).
Informació revisada al novembre de 2023.


