La leucemia linfoblástica aguda infantil de tipo T
La leucemia es el cáncer más frecuente en niños. Afecta a más de 350 peques al año en nuestro país, un tercio son menores de 4 años. La leucemia representa el 30% de todos los cánceres pediátricos, siendo la leucemia linfoblástica aguda B, la forma más común en niños (80% de los casos)
La información proporcionada en www.fcarreras.org sirve para apoyar, no reemplazar, la relación que existe entre los pacientes/visitantes de este sitio web y su médico.

¿Qué es la leucemia, la médula ósea y cuáles son los tipos de células sanguíneas?
La leucemia es un tipo de cáncer de las células de la sangre y de la médula ósea. Ver apartado Leucemia, médula ósea y células sanguíneas.
¿Qué es la leucemia linfoblástica aguda T?
 La leucemia linfoblástica aguda (LLA) es un tipo de cáncer por el que la médula ósea produce demasiados linfocitos inmaduros (tipo de glóbulo blanco), conocidos como linfoblastos. Estas células impiden el del resto de células de la sangre. La LLA es el cáncer más frecuente en niños y la mayoría de los diagnósticos son de leucemia linfoblástica aguda B (80% de los casos de leucemia en niños). La leucemia linfoblástica T es un subtipo de la enfermedad heterogéneo y raro que afecta a pocos niños al año en España. Supone el 10-15% de los casos de LLA en niños.
La leucemia linfoblástica aguda (LLA) es un tipo de cáncer por el que la médula ósea produce demasiados linfocitos inmaduros (tipo de glóbulo blanco), conocidos como linfoblastos. Estas células impiden el del resto de células de la sangre. La LLA es el cáncer más frecuente en niños y la mayoría de los diagnósticos son de leucemia linfoblástica aguda B (80% de los casos de leucemia en niños). La leucemia linfoblástica T es un subtipo de la enfermedad heterogéneo y raro que afecta a pocos niños al año en España. Supone el 10-15% de los casos de LLA en niños.
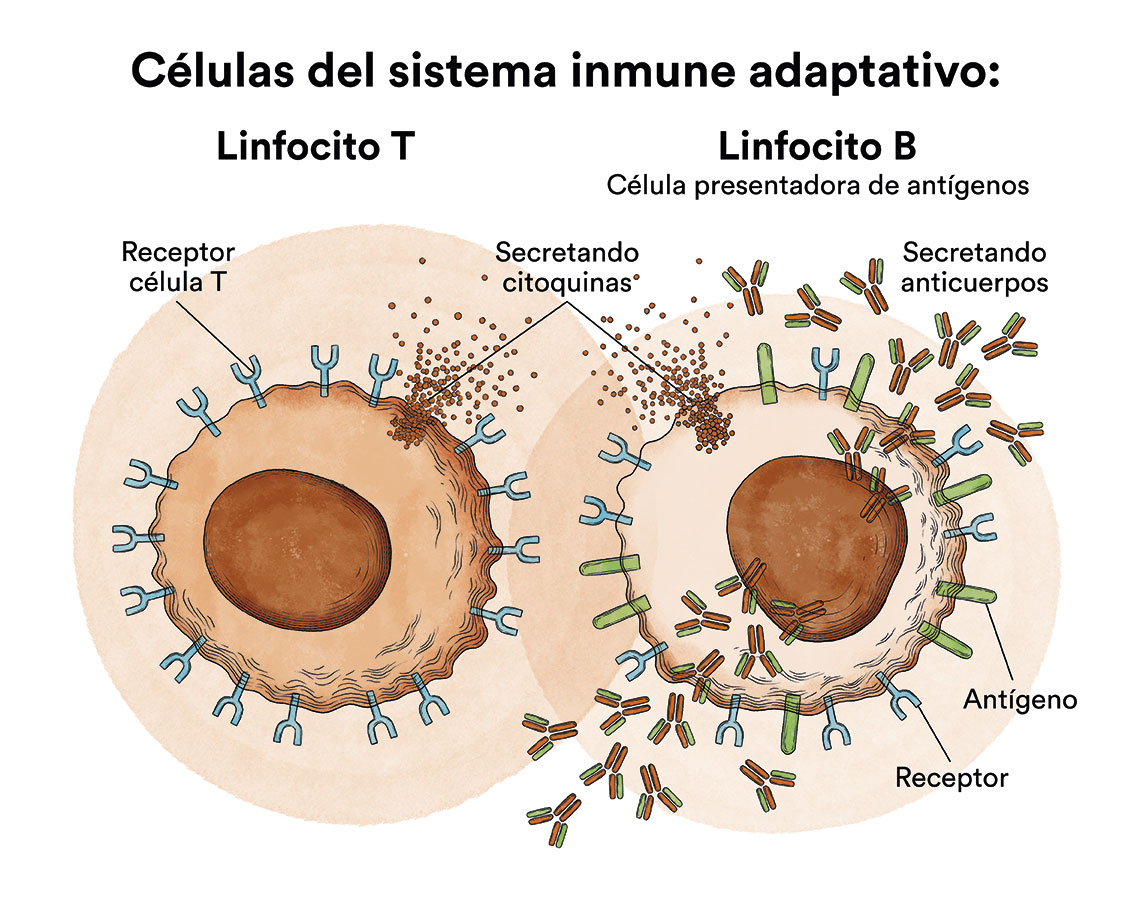
Los linfocitos son un tipo de leucocitos o glóbulos blancos y pueden ser de dos tipos, B y T. Según los linfoblastos se originen de células B o T, la LLA se denominará de LLA- B o LLA- T.
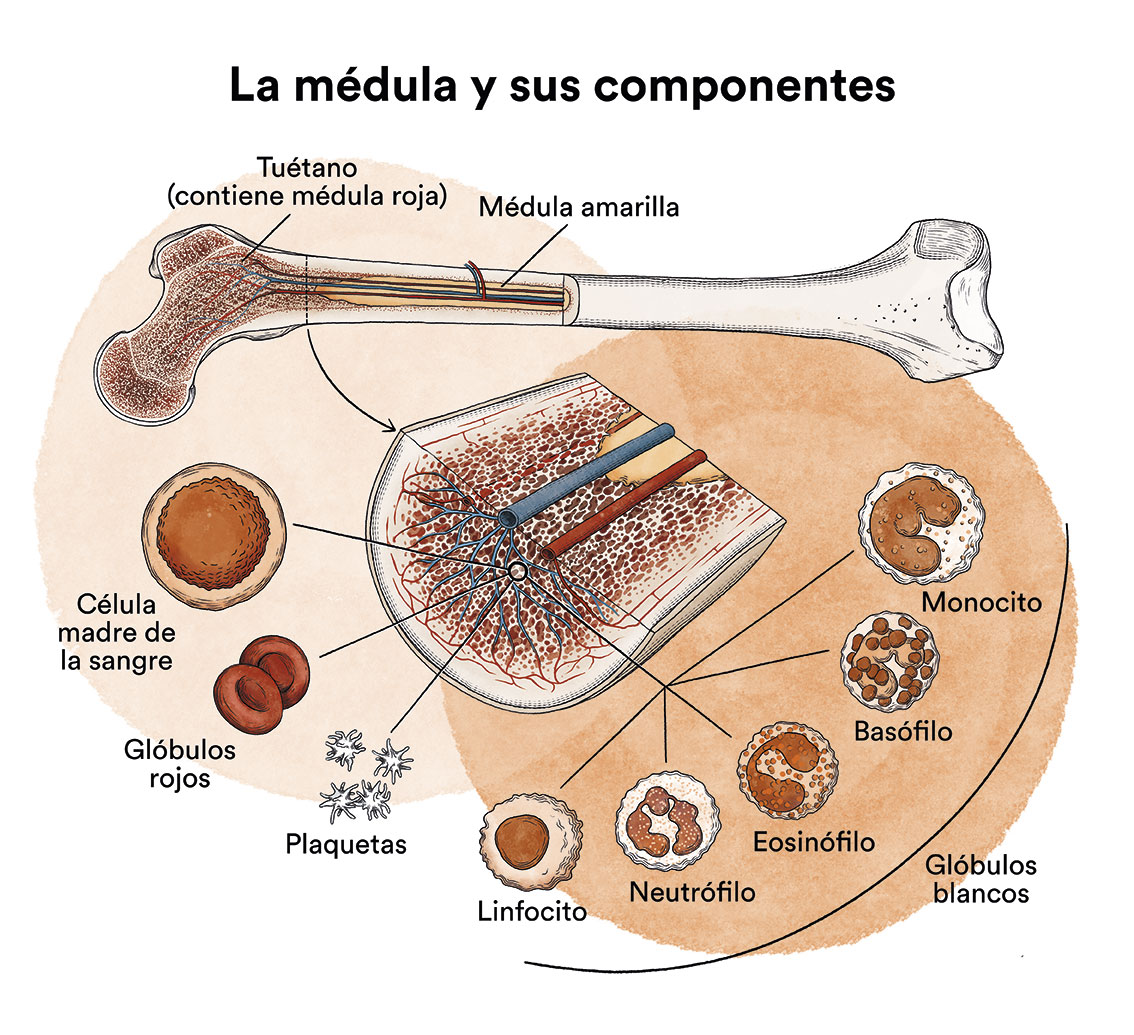
Como hemos visto en ‘Leucemia, médula ósea y células sanguíneas’, la médula ósea elabora las células madre sanguíneas (células inmaduras) que, con el tiempo, se transformarán en células sanguíneas maduras. Una célula madre sanguínea se convierte en una célula madre mieloide o en una célula madre linfoide.
Una célula madre mieloide se convierte en uno de los tres tipos de glóbulos sanguíneos maduros:
- Glóbulos rojos, que transportan el oxígeno a otros tijos y
órganos del cuerpo - Granulocitos, glóbulos blancos que ayudan a combatir infecciones
y otras enfermedades - Plaquetas, que colaboran en la coagulación de la sangre cuando se
produce la rotura de un vaso sanguíneo.
- Glóbulos rojos, que transportan el oxígeno a otros tijos y
Una célula madre linfoide se convierte en un linfoblasto y, más tarde, en uno de los tres tipos de linfocitos (glóbulos blancos):
- linfocitos B, que producen anticuerpos para ayudar a combatir las infecciones del cuerpo
- linfocitos T, que ayudan a los linfocitos B a producir anticuerpos para combatir infecciones
- linfocitos citolíticos naturales o linfocitos NK (natural killer), un tipo de célula inmunitaria que contiene enzimas que pueden destruir células tumorales o células infectadas por virus.
En los niños afectados por una leucemia linfoblástica aguda B, hay demasiadas células madre que se transforman en linfoblastos T.
¿Cuáles son las causas de la leucemia linfoblástica aguda T?
Se desconoce la causa exacta que origina la LLA-T. La investigación en este campo es importante y se van conociendo los cambios genéticos que suceden en las células leucémicas.
Sin embargo, en la mayoría de los niños con LLA- T se desconoce cuáles son los desencadenantes o los factores que le han originado la leucemia.
En una minoría de niños sí existen algunas enfermedades genéticas que les predispone al desarrollo de la leucemia linfoblástica aguda. Este es el caso de niños con síndrome de Down o con otros síndromes como el síndrome de Li-Fraumeni, la ataxia-telangiectasia, la Anemia de Fanconi y otros. Otros factores que aumentan la posibilidad de padecer una leucemia pueden ser la exposición a radiaciones previo al nacimiento (radiografías) o haber recibido quimioterapia por otro cáncer
Los hermanos de un niño con leucemia, comparados con otros niños, tienen un pequeño aumento del riesgo de padecer leucemia. Sin embargo, este riesgo es muy bajo, inferior a 1 por mil.
La leucemia, como otros tipos de cáncer, no es contagiosa. Ver apartado Leucemia, médula ósea y células sanguíneas.
¿Cuáles son los síntomas de la leucemia linfoblástica aguda T?
- Cansancio y palidez (por anemia)
- Aparición de morados y pequeñas manchas rosadas en la piel (petequias) u otros sangrados (por un recuento de plaquetas bajo)
- Fiebre e infecciones que no evolucionan bien (debido al mal funcionamiento de los leucocitos)
- Dolor en las articulaciones y los huesos o cojera (por la invasión de la médula ósea por las células leucémicas)
- Adenopatías o aumento de tamaño de los ganglios linfáticos (por ocupación de las células leucémicas en el sistema linfático)
 Al inicio de la enfermedad, todos estos síntomas pueden ser muy parecidos a los de una infección por un virus. Cuando los síntomas continúan más de 2-4 semanas, en una mayoría de casos se puede llegar a el diagnóstico. Como no son síntomas específicos o exclusivos de la leucemia, es muy frecuente que se haya consultado en diversas ocasiones al médico antes de que se llegue al diagnóstico. Generalmente, esto no influye en las opciones de curación del niño o niña.
Al inicio de la enfermedad, todos estos síntomas pueden ser muy parecidos a los de una infección por un virus. Cuando los síntomas continúan más de 2-4 semanas, en una mayoría de casos se puede llegar a el diagnóstico. Como no son síntomas específicos o exclusivos de la leucemia, es muy frecuente que se haya consultado en diversas ocasiones al médico antes de que se llegue al diagnóstico. Generalmente, esto no influye en las opciones de curación del niño o niña.¿Cómo se diagnostica la leucemia linfoblástica aguda T?
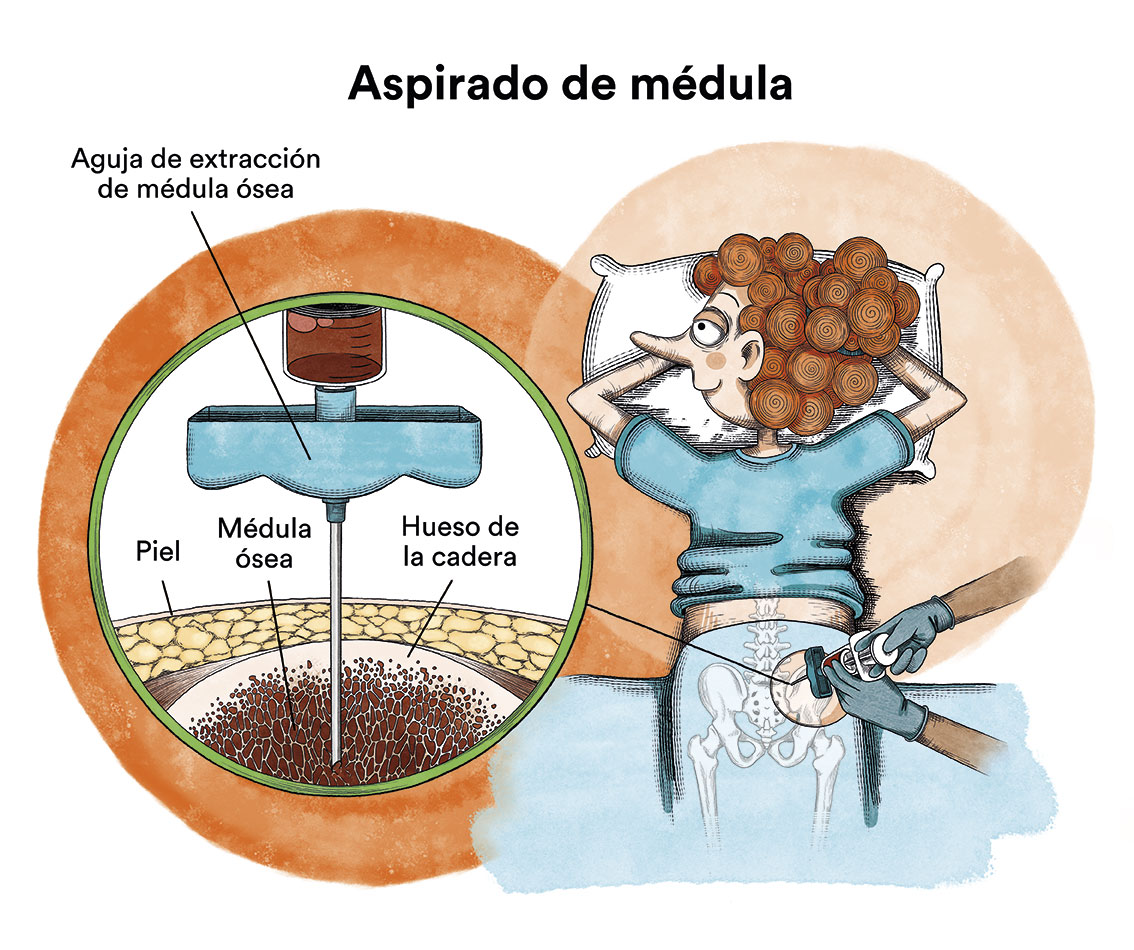
Generalmente, si un niño presenta los síntomas característicos, la leucemia se puede diagnosticar con una analítica sanguínea. Al examinar la sangre por el microscopio, se pueden ver células leucémicas. A veces, al comienzo de la enfermedad, estas células no se ven en la sangre y la leucemia se sospecha por los síntomas y algunas alteraciones en la analítica sanguínea. El diagnóstico se confirma mediante una punción médula ósea (crestas ilíacas) y análisis de las células obtenidas.
¿Cuál es el tratamiento de la leucemia linfoblástica aguda T en niños?
El tratamiento de la leucemia linfoblástica aguda infantil de células T (LLA-T) recién diagnosticada en las fases de inducción a la remisión, consolidación e intensificación y mantenimiento siempre incluye quimioterapia combinada. A los niños con LLA-T, se les administran más medicamentos contra el cáncer y en dosis más altas que a los niños del grupo de riesgo estándar con diagnóstico reciente, aunque en el momento actual se utilizan los mismos fármacos y esquemas de quimioterapia que para la leucemia linfoblástica aguda B.

Se administra quimioterapia intratecal y sistémica para prevenir o tratar la diseminación de las células leucémicas al encéfalo y la médula espinal. Algunas veces, también se administra radioterapia dirigida al encéfalo.
El objetivo del tratamiento de la leucemia linfoblástica aguda es eliminar las células leucémicas para permitir que la médula ósea vuelva a trabajar con normalidad.
El equipo de médicos hematólogos del niño decidirá cuál es el mejor tratamiento para él, teniendo en cuenta muchos factores, entre los que destacan:
- el tipo de LLA que tiene (B o T)
- la edad del niño y el número de leucocitos al diagnóstico
- las características genéticas de las células leucémicas
- la respuesta que presente al tratamiento
El tratamiento de la LLA sigue protocolos de tratamiento elaborados por especialistas en hematología y oncología pediátrica y están basados en resultados de otros protocolos (de grupos nacionales e internacionales).
La quimioterapia es el principal tratamiento que recibirá el niño. Consiste en la utilización de medicamentos que eliminan las células cancerosas impidiendo que se reproduzcan.
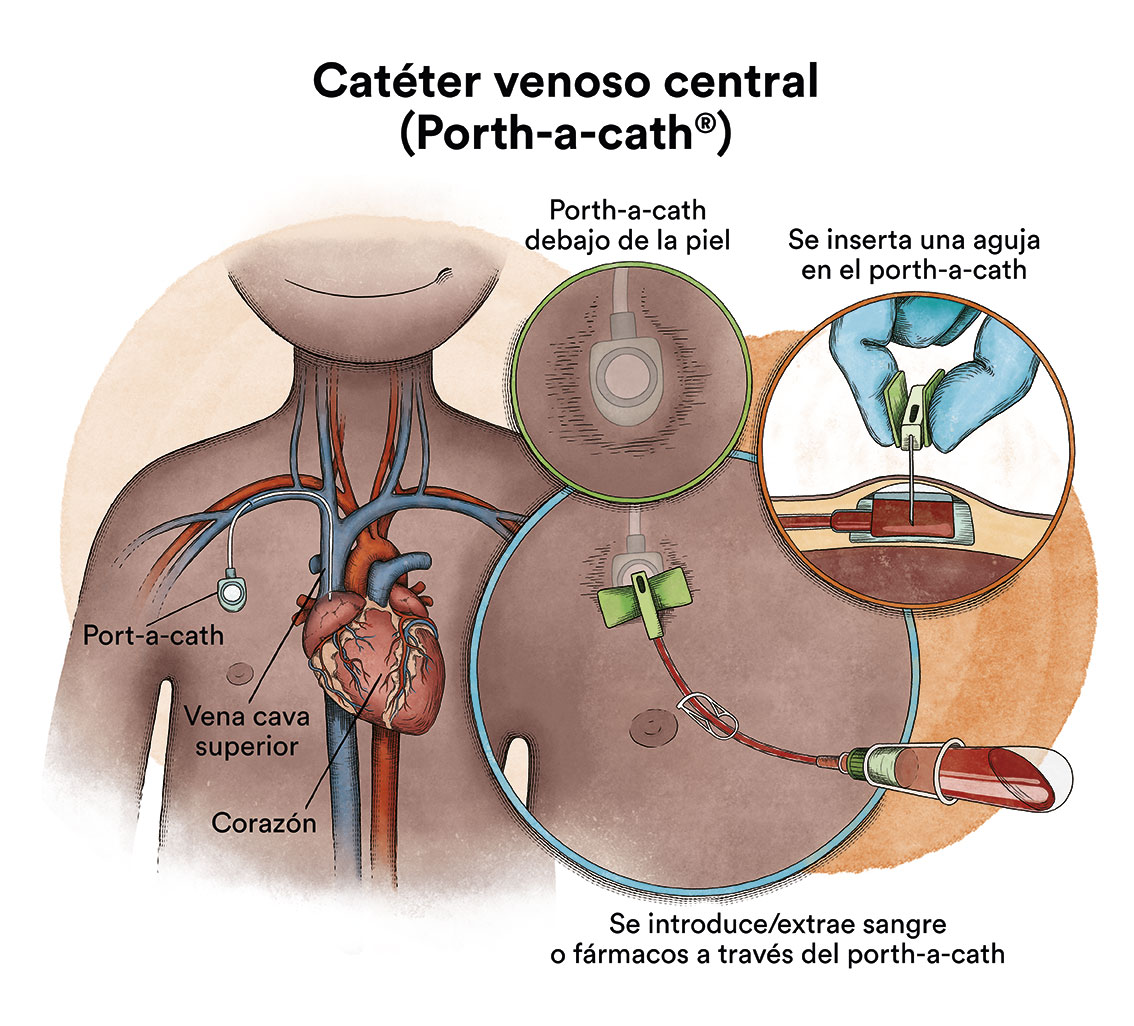
Cuando la quimioterapia se administra por vía intravenosa, para evitar pinchar repetidamente una vena, se utiliza un dispositivo especial llamado catéter. El catéter se introduce en una vena grande que permite administrar todo tipo de medicamentos, así como también extraer sangre para los análisis de sangre, evitando las repetidas punciones al niño.
Existe un tipo de catéter, llamado port-a-cath, que se une a un reservorio redondo de plástico o metal que queda bajo la piel del tórax. El port-a-cath es muy práctico en niños porque al quedar bajo la piel no permite que el niño se lo arranque, es más difícil que se infecte que otros tipos de catéter y permite que el niño se bañe.
Si la quimioterapia se administra por un catéter venoso llega, por la sangre, a la casi totalidad de las células del cuerpo. Sin embargo, la mayoría de los medicamentos de la quimioterapia no llegan bien al líquido cefalorraquídeo que baña el cerebro y médula espinal. Esto hace que haya células leucémicas que pueden sobrevivir en este líquido. Con el fin de prevenir que las células leucémicas que llegan al líquido cefalorraquídeo sobrevivan y sean la causa de una futura recaída al sistema nervioso, se debe administrar quimioterapia directamente en el líquido cefalorraquídeo, mediante punciones lumbares (quimioterapia intratecal). En una minoría de niños que por las características de su LLA sabemos que tienen más riesgo de recaída en el sistema nervioso, este tratamiento se puede complementar con radioterapia craneal.
El tratamiento con quimioterapia puede curar hasta un 85-90% de los niños con LLA-T. Cuando no se observan células de la leucemia en la médula ósea ni en ningún otro lugar se dice que el paciente está en remisión completa. El pronóstico de la ALL de células T no resulta muy afectado por la edad del paciente. Existe un subtipo de la enfermedad especial de mal pronóstico que está siendo investigado. Se trata de la LLA early pre-T que corresponden al 12% de todas las LLA-T), para el cual se están evaluando quimioterapias con actividad mixta (mieloide y linfoide), así como nuevos fármacos en el seno de ensayos clínicos. En este caso se recomienda un trasplante de médula ósea para todos los pacientes. Actualmente se precisan más estudios para establecer recomendaciones terapéuticas de estos casos en la infancia. En el protocolo actual para las early pre-T (TOTAL XVII St Jude Children’s Research Hospital) se intensifica su tratamiento y se añade el fármaco ruxolitinib.
En general, un 15-20% de los niños pueden recaer de la leucemia. La mayoría de las recaídas tienen lugar en los primeros 5 años desde el diagnóstico, en especial en los primeros 2 años tras haber finalizado el tratamiento. En los casos que hay una recaída, se vuelve a administrar quimioterapia y, según el caso, se realiza un trasplante de médula ósea (ver LLA RECAÍDA). También existen nuevas modalidades de tratamiento para los niños en recaída (ver NUEVOS TRATAMIENTOS)
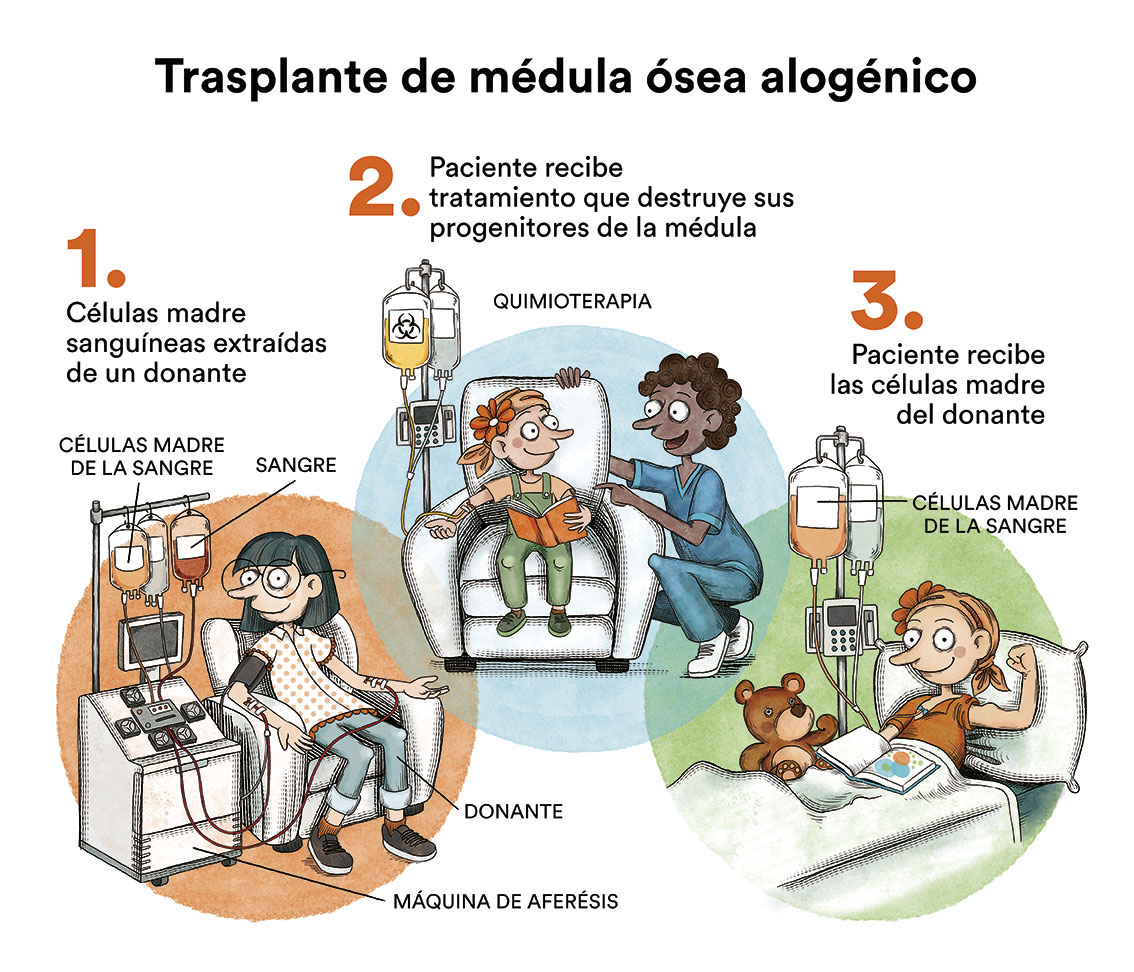
El trasplante se reserva para los casos más difíciles de curar con sólo quimioterapia dado que es un tratamiento más intensivo y que tiene más riesgos y posibles secuelas.
En los niños que han recaído o en aquellos que, por las características de su leucemia, sabemos que tienen un riesgo muy alto de recaer, sí está indicado realizar un trasplante de médula ósea. Este se hace una vez se ha alcanzado una nueva remisión completa con quimioterapia intensiva u otras modalidades de tratamiento. Con el trasplante, las posibilidades de curación pueden aumentar.
Jorge
Leucemia linfoblástica aguda.
“Jorge fue diagnosticado de leucemia linfoblástica aguda cuando era muy pequeño. En su casa siempre decían que Jorge había llegado ‘de regalo’ cuando sus padres querían tener una hermanita para su hijo mayor, Pablo. Y así llegaron los mellizos: Lucía y Jorge. Lo que descubrieron con el tiempo es que el verdadero regalo había sido Lucía, ya que era 100% compatible con Jorge, que necesitaba un trasplante de médula ósea para curarse. El trasplante no fue fácil y, obviamente, pasaron todo mucho miedo. Pero como dice Fran, su mamá, Jorge cruzó la meta. Y años más tarde puede decirle que los superhéroes como él ya le han ganado una vez la partida a la vida. Ahora toca ser y hacer lo que se proponga. Ya han pasado 10 años de su trasplante y Jorge está genial”.
¿Qué probabilidades tienen de curarse los niños con leucemia linfoblástica aguda T?

¿Qué ocurre si el niño recae?
Si el niño sufre una recaída de la leucemia linfoblástica aguda, las posibilidades de curación y el tratamiento dependerán de varios factores, fundamentalmente:
- del tiempo transcurrido entre el diagnóstico y la recaída, cuando más tiempo, mejor
- de si se trata de una leucemia linfoblástica aguda de tipo B o T
- de la localización de la recaída (médula ósea u otros como el sistema nervioso, testículos u otros)
- la respuesta que tenga al tratamiento de la recaída
El tratamiento generalmente consistirá en quimioterapia más intensiva que la recibida inicialmente y, a menudo, trasplante de médula ósea.
En los últimos años, además de la quimioterapia, existen nuevos tratamientos que pueden sustituir o complementar a la quimioterapia, como la inmunoterapia y los tratamientos dirigidos contra una diana molecular (Ver NUEVOS TRATAMIENTOS).
Nuevos tratamientos contra la leucemia linfoblástica aguda T
En los últimos años se está produciendo una revolución en el tratamiento del cáncer y de la leucemia linfoblástica aguda B específicamente. Entre los nuevos tratamientos que hay disponibles para tratar la LLA-B destacan los tratamientos conocidos como medicina de precisión y la inmunoterapia, especialmente la inmunoterapia CAR-T.
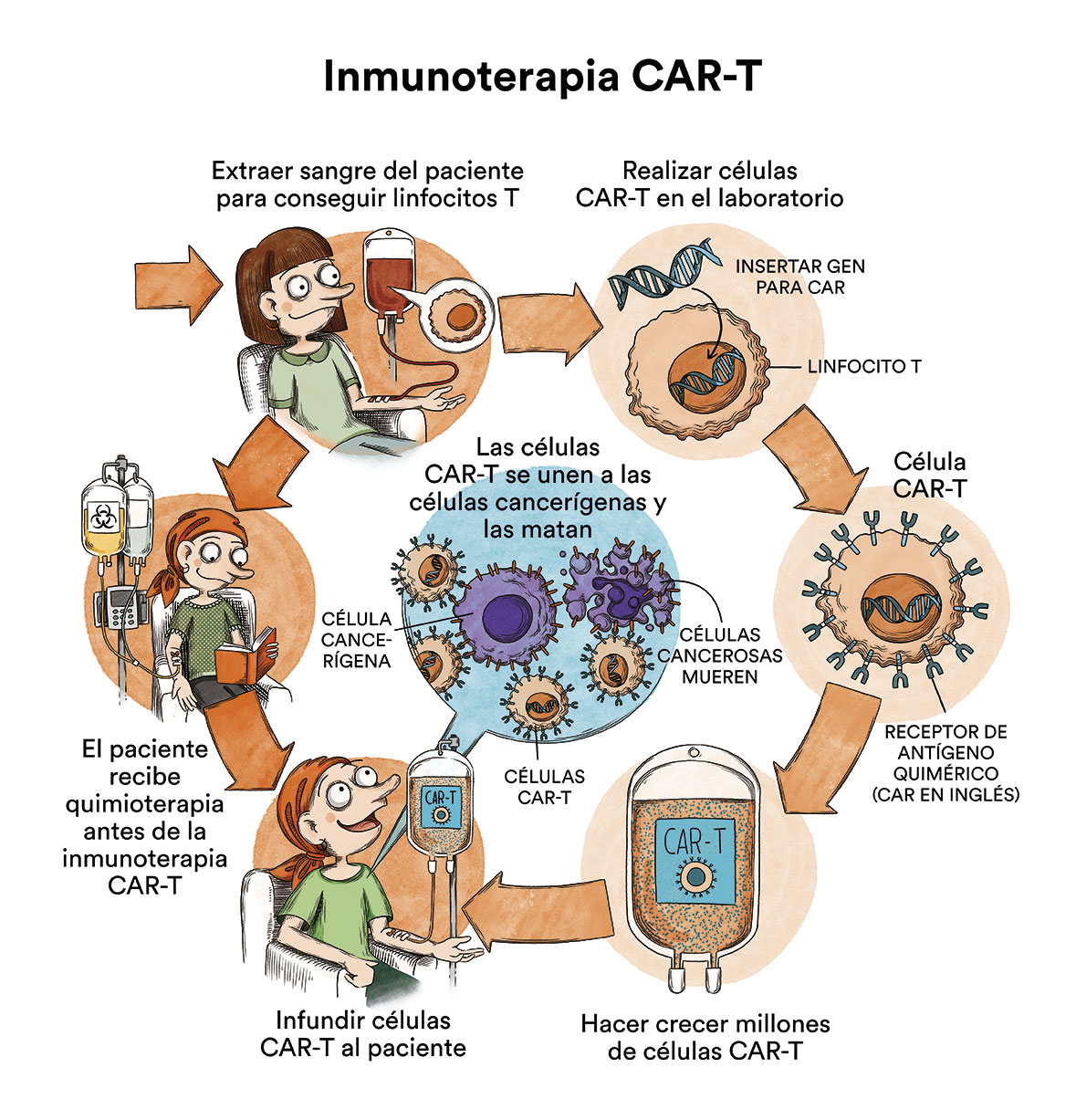
 A pesar de ello, también se están produciendo avances en forma de ensayos clínicos para las LLA-T.
A pesar de ello, también se están produciendo avances en forma de ensayos clínicos para las LLA-T.
En el caso de recaídas, la nelarabina es actualmente el único fármaco con aprobación, aunque su eficacia es limitada y puede conllevar efectos secundarios graves. Aunque se están valorando actualmente ensayos clínicos con terapias dirigidas a dianas (venetoclax, navitoclax, inhibidores de JAK, entre otros), asociadas o no a quimioterapias.
Los tratamientos de inmunoterapia son tratamientos contra el cáncer que ayudan al sistema inmunitario a combatir el cáncer. El propio sistema inmunitario es potenciado para ayudar a su cuerpo a combatir las infecciones y otras enfermedades. La inmunoterapia se puede utilizar sola o en combinación con quimioterapia u otros tratamientos contra el cáncer.
Entre otras terapias celulares, el tratamiento con linfocitos T CAR (CAR-T cells) ha tenido resultados muy prometedores en niños con LLA de tipo B. Los linfocitos T CAR son linfocitos que se recogen del paciente y se los modifica genéticamente para que reconozcan y destruyan a la célula leucémica. Ver Inmunoterapia CAR-T o cómo rediseñar las propias células para atacar el cáncer En pacientes con leucemias T, la estrategia de inmunoterapia cuenta con la complejidad e inconveniente de que las propias células T (las que se modifican para atacar al cáncer) son las que están enfermas. A pesar de ello, se están desarrollando estrategias de CAR-T, todavía en forma de ensayos clínicos, contra los antígenos CD7, CD5 o CD1a para la LLA-T tímica cortical). Éstas pueden resultar prometedoras con el tiempo.
Actualmente, para poder realizar inmunoterapias CAR-T en pacientes con leucemias linfoblásticas de tipo T, se están desarrollando una terapia llamada STAb que se basa en la secreción de un tipo especial de anticuerpo denominado biespecífico que puede reconocer dos dianas, una en la célula tumoral y otra en la célula T. De esta forma los anticuerpos biespecíficos crean una especie de puente artificial que pone en contacto las células T terapéuticas con las células tumorales, facilitando la eliminación de estas últimas y manteniendo a salvo los linfocitos T sanos.
Esta distinción es fundamental para poder tratar la leucemia aguda linfoblástica de células T. En el caso de la leucemia linfoblástica aguda de células B (LLA-B) las células CAR-T al reconocer una sola diana, destruyen tanto las células B enfermas como las sanas, aunque estos pacientes pueden llevar una vida normal gracias al aporte periódico de inmunoglobulinas –anticuerpos- obtenidos de donantes sanos.
En las LLA-T es más difícil aplicar una terapia CAR-T, ya que las células que se emplean para combatir al tumor -linfocitos T- son las mismas que están enfermas y su uso puede originar un estado de inmunodeficiencia incompatible con la vida. Además, no existe una terapia de sustitución disponible como sí ocurre en las leucemias de células B.
Seguimiento
Recomendaciones y otros aspectos prácticos
A continuación, hacemos unas recomendaciones de carácter general y que responden a algunas de las preguntas más frecuentes que realizan los padres de los niños con leucemia:
- ¿Se le caerá el pelo? ¿Cuándo? ¿Lo debemos cortar?
Con la quimioterapia que recibirá para tratar la leucemia, el cabello se le caerá. Generalmente, esto sucede a las 2-3 semanas del inicio de la quimioterapia. Si el niño o la niña tiene el pelo largo, es más adecuado cortarlo corto antes de que empiece a caer. No es necesario, ni conveniente desde el punto de vista psicológico, cortarlo durante los primeros días del ingreso. Tampoco hay que explicarle este hecho en un primer momento. Sí conviene, sin embargo, abordar este tema con el niño antes de que empiece a caer. El cabello vuelve a salir al cabo de 2-4 semanas de haber iniciado la fase de tratamiento de mantenimiento, en la que la quimioterapia es de menor intensidad.
- Higiene
Debido a que el niño tiene disminuidas sus defensas ante las infecciones (por la propia enfermedad y también por el tratamiento administrado), es conveniente mantener una higiene corporal adecuada del niño, de la habitación del hospital y del domicilio familiar, así como de sus juguetes.
Es recomendable evitar aquellos juguetes que almacenen mucho polvo y las cajas de cartón. Tampoco se ha de almacenar comida fuera del frigorífico. Las plantas están prohibidas en la habitación, ya que en la tierra hay esporas de hongos.
El orden facilita la limpieza por parte del personal de la limpieza del hospital.
- Visitas
Es conveniente reducir el número de visitas en la habitación del niño, ya que pueden ser portadoras de infecciones. Es recomendable que no haya más de 2 acompañantes en la habitación y que se laven las manos antes de entrar. Si alguno de los visitantes tiene algún proceso infeccioso (resfriado, conjuntivitis …) es preferible que no venga.
En el caso de que éste sea el padre, la madre u otra persona que cuide del niño y que no se pueda prescindir de su atención, convendría que se pusieran una mascarilla y se lavaran las manos antes de entrar en contacto con el niño.
- Alimentación
El niño que recibe tratamiento con quimioterapia intensiva debe recibir una alimentación variada. Es conveniente, cuando la cifra de leucocitos es baja, evitar los alimentos crudos que no se puedan pelar (por ejemplo: lechuga, fresas, tomate crudo).
En ocasiones la quimioterapia puede quitar el hambre, o incluso provocar náuseas. Durante los días que esté recibiendo la quimioterapia, no conviene forzar al niño para que coma, porque puede ser contraproducente.
Por otro lado, los corticoides (prednisona y dexametasona) que recibirá en algunas fases del tratamiento pueden aumentar mucho el apetito, incluso con ansiedad. Si bien se les puede permitir comer algo más que las comidas que se sirven en el hospital, no se les debe dejar comer sin límite, ya que con frecuencia no lo toleran bien y puede ocasionar dolor de estómago.
Enlaces de interés sobre temas médicos relacionados con la leucemia linfoblástica aguda en niños
- Tratamiento de la leucemia linfoblástica aguda en niños. National Cancer Institute.
- Leucemia linfoblástica aguda en niños y adolescentes. St Jude International
Enlaces de interés sobre otros temas relacionados con la leucemia linfoblástica aguda en niños
MATERIALES LEUCEMIA INFANTIL
- Los bebés también tienen leucemia. Fundación Josep Carreras contra la leucemia.
- Leucemia infantil. Los pequeños imparables. Fundación Josep Carrerascontra la leucemia.
- Juego recortable Medulín. Fundación Josep Carreras contra la leucemia.
La Fundación Josep Carreras dispone de un cuento “El bebé forzudo” dirigido a niños o hermanos que padecen leucemia. Está especialmente dirigido a niños hasta los 6 años. Si quieres solicitarlo, puedes enviarnos un correo a imparables@fcarreras.es.
TRASPLANTE DE MÉDULA ÓSEA
- Guía del Trasplante de Médula Ósea. Fundación Josep Carreras contra la leucemia.
- ¿Qué es el HLA y cómo funciona? Fundación Josep Carreras contra la leucemia.
- La Enfermedad Injerto contra Receptor Fundación Josep Carreras contra la leucemia.
- Historia del Trasplante de Médula Ósea. Fundación Josep Carreras contra la leucemia.
- ¿Cómo se realiza la búsqueda de un donante compatible anónimo? Fundación Josep Carreras contra la leucemia.
- Guía de cuidados para niños trasplantados. TransplantCHild.
- El trasplante de células madre: un libro para colorear. Leukeamia and Lymphoma Society.
MANUALES DE APOYO
- ¿Cómo enfrentarse a la leucemia y el linfoma en niños? Leukemia & Lymphoma Society.
- VIVIR APRENDIENDO. Protocolo de actuación para alumnos con cáncer AFANION.
- Guía de apoyo para padres de niños oncológicos ASION.
- Guía para jóvenes y adolescentes con cáncer ASION.
- Alumnado con cáncer. guía para docentes ASION.
- La importancia del comportamiento de los padres cuando un niño tiene cáncer ASION.
- Mi hijo tiene cáncer. ¿Qué hago? FARO.
ALIMENTACIÓN
- ¿Cómo mantener una alimentación saludable durante el tratamiento? Fundación Josep Carreras contra la leucemia.
- “Buen provecho”. Consejos dietéticos durante el tratamiento AFANION.
- ‘Las recetas mágicas de Jabel’. Isabel Rojas Murcia, Carolina Mangas Gallardo.
OTROS
- Información sobre los efectos a largo plazo y tardíos del tratamiento para la leucemia o el linfoma en los niños Leukemia & Lymphoma Society.
- Mi hermano tiene cáncer Fundación Josep Carreras contra la leucemia.
- La escuela en un hospital Fundación Josep Carreras contra la leucemia.
- Educando ilusiones. Guía para la intervención psicoeducativa en niños y adolescentes con cáncer FARO.
- El cáncer en la adolescencia Fundación Josep Carreras contra la leucemia.
- Documental ‘La leucemia y los adolescentes’ Fundación Josep Carreras contra la leucemia.
- Documental ‘Los bebés también tienen leucemia’ Fundación Josep Carreras contra la leucemia.
- 7 formas de ponerse un pañuelo Fundación Josep Carreras contra la leucemia.
- Cuento ‘La princesa Luzie y los caballeros de la quimio’ ASPANAFOA.
- Cuento ‘Vamos a quimioterapia’.
- Cuento ‘Vamos a radioterapia’.
- Cuento ‘Gasparín Super Quimio’ Federación Española de Padres de Niños con Cáncer.
- Vídeo ‘Charlie Brown y la leucemia’.
- Cuento ‘Toby y la máquina voladora’.
- Cuento ‘El hada de las estrellas’ AECC.
- Cuento ‘Lina la pequeña golondrina’ Osakidetza.
Enlaces de interés: entidades locales (recursos y servicios)
Apoyo y ayuda
Te invitamos también a seguirnos a través de nuestras redes sociales principales (Facebook, Twitter e Instagram) en las que, a menudo, compartimos testimonios de superación.
Si resides en España, también puedes ponerte en contacto con nosotros enviándonos un correo electrónico a imparables@fcarreras.es para que te ayudemos a ponerte en contacto con otras familias que han superado esta enfermedad.
* De acuerdo con la Ley 34/2002 de Servicios de la Sociedad de la Información y el Comercio Electrónico (LSSICE), la Fundación Josep Carreras contra la Leucemia informa que toda la información médica disponible en www.fcarreras.org ha sido revisada y acreditada por el Dr. Enric Carreras Pons, Colegiado nº 9438, Barcelona, Doctor en Medicina y Cirugía, Especialista en Medicina Interna, Especialista en Hematología y Hemoterapia y Consultor senior de la Fundación; y por la Dra. Rocío Parody Porras, Colegiada nº 35205, Barcelona, Doctora en Medicina y Cirugía, Especialista en Hematología y Hemoterapia y adscrita a la Dirección médica del Registro de Donantes de Médula Ósea (REDMO) de la Fundación).
Información revisada en noviembre de 2023.


